デンカ(株)、インフルエンザウイルス抗原迅速診断キットの一部変更承認を取得、検査体制の充実に期待
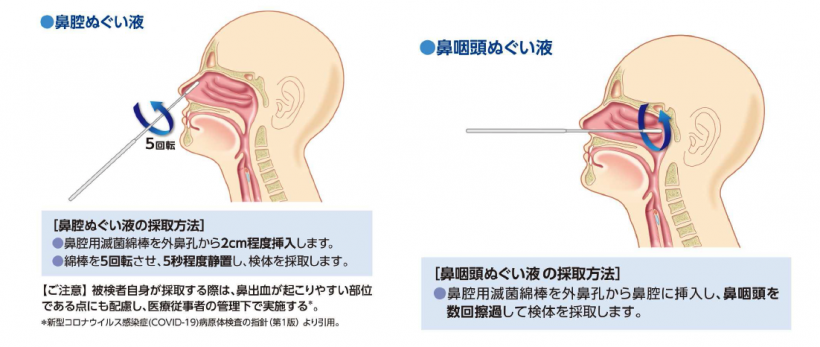
デンカ株式会社(東京都中央区)は30日、インフルエンザウイルス抗原診断キット「クイックナビ™-Flu2」の製造販売承認事項一部変更(※)承認を厚生労働省より30日付で受けた、と発表した。この承認により、一般社団法人日本感染症学会からの提言で推奨されている新型コロナウイルスとインフルエンザウイルスの同時検査を行う際に鼻腔ぬぐい液も共用できることが明確化され、一般の医療機関での検査体制拡充が期待される。
併せて、鼻腔ぬぐい液について、クイックナビ™-Flu2も、クイックナビ™-COVID19Agと同様に、医療従事者の管理のもと受診者による検体採取が可能となった。これにより、医療従事者の感染リスクがさらに低減されるほか、受診者の負担軽減にもつながる。
一部変更承認は販売提携先の大塚製薬株式会社(本東京都千代田区)から販売される製品にも適用されます。
(※)変更内容 従来の適用検体種表記:「鼻腔拭い液」→ 変更後の表記:「鼻咽頭ぬぐい液と鼻腔ぬぐい液」